Conferencia Episcopal
Peruana
Anticoncepci¾n Oral de
Emergencia: Mecanismos de Acci¾n
- Documentaci¾n CientĒfica
-
INFORME DEL COMIT╔ DE
BIOETICA
Lima 19 de Julio del
2004
Contenidos.
Lista de los Anexos.
Estudios
Realizados por la OMS.
Revisiones de la
Anticoncepci¾n de Emergencia.
Estudios que
Demuestran Cambios Endometriales.
Estudios que no
encuentran el tercer mecanismo con el uso de LNG.
Otros Documentos Anexados.
I. Introducci¾n.
II.
Preliminares.
A. Condiciones
requeridas por el Ministerio de Justicia.
B. Los
mecanismos de acci¾n del levonorgestrel 0.75mg:
III. Sobre la primera condici¾n puesta por el
Ministro de Justicia:
A. La Evidencia
Experimental.
B. recogida por
la comunidad cientĒfica.
IV.
Sobre la segunda condici¾n puesta por el Ministro de Justicia.
A. Estudios
cientĒficos sĒ encuentran cambios endometriales.
B. Los artĒculos
citados en el debate sobre el mecanismo de acci¾n del levonorgestrel no
demuestran que la AOE no tenga efecto sobre el endometrio.
C. Deficiencias
del Informe Tßvara.
V. Otras
Opiniones a Considerar
VI.
Conclusi¾n:
VII.
Bibliografia.
--------------------------------------------------------------------------------
Lista de los Anexos
Estudios Realizados por la
OMS
1. WHO Task Force on Postovulatory Methods of Fertility Regulation. Randomised controlled trial of levonorgestrel versus the Yuzpe regimen of combined oral contraceptives for emergency contraception. Lancet 1998;352:428-433.
2. WHO
Research Group on Post-ovulatory Methods of Fertility Regulation. Published. von
Hertzen H, Piaggio G, Ding J, et al. Low dose mifepristone and two regimens of
levonorgestrel for emergency contraception: a WHO multicentre randomized trial.
Lancet. 2002;
360:1803-1810.
Revisiones de la Anticoncepci¾n de Emergencia
1.
Gemzell-Danielsson K, Marions L., Mechanisms of action of mifepristone
and levonorgestrel when used for emergency contraception. Hum Reprod Update.2004
Jul-Aug;10(4):341-8. (Abstract).
2. Sarkar
NN., Levonorgestrel as an emergency contraceptive drug.
Int J Clin
Pract. 2003 Nov;57(9):824-8.
3. Croxatto
HB, Ortiz ME, Muller AL., Steroids. Mechanisms of action of emergency
contraception. 2003 Nov;68(10-13):1095-8.
4. Kahlenborn
C, Stanford JB, Larimore WL. Postfertilization effect of hormonal emergency
contraception. Ann Pharmacother. 2002 Mar;36(3):465-70.
5. Grimes DA,
Raymond E., Emergency Contraception. Ann Intern Med 2002 ; 137
:180-9
6. Pham A.
Emergency contraception (post-coital Contraception), J Okla State Med Assoc.
2002 Jun;95(6):371-4. (Abstract).
7. Croxatto
HB, Devoto L, Durand M, Ezcurra E, Larrea F, Nagle C, Ortiz ME, Vantman D, Vega
M, von Hertzen H. Mechanism of action of hormonal preparations used for
emergency contraception: a review of the literature. Contraception. 2001
Mar;63(3):111-21. Review. No abstract available.
8. Wertheimer
RE. Emergency postcoital contraception.Am Fam Physician. 2000 Nov 15;62(10):2287-92.
Review.
Estudios que Demuestran Cambios Endometriales
1. Moggia A,
Beauquis A, Ferrari F, Torrado ML, Alonso JL, Koremblit E, Mischler T. The use
of progestogens as postcoital oral contraceptives.
Reprod Med. 1974
Aug;13(2):58-61
2. Ugocsai G,
Resch B, Traub A, Sas M., Biological, microscopic and scanning electron
microscopic investigations of the effects of postinor /d-norgestrel/ in rabbits.
Contraception. 1984 Aug;30(2):153-9.
3. Ugocsai
G., Pozsa M, Ugocsai P. Scanning electron microscopic (SEM) changes of the
endometrium in women takimg high doses of levonorgestrel as emergency postcoital
contraception Contraception 2002 Dec; 66(6): 433-7.
4. Landgren
BM, Johanisson E, Aedo AR, Kumar A, Shi Yong-en.
The effect of
Levonorgestrel administered in large doses at different stages of the cycle on
ovarian function and endometrial morphology. Contraception, 39 (3), 1989. 275-
289.
5. Shirley B,
Bundren JC, McKinney S.
Levonorgestrel
as a postcoital contraceptive. Contraception. 1995
Nov;52(5):277-81.
6. Roopa BA,
Loganath A, Singh K. Hum Reprod. The effect of a levonorgestrel-releasing
intrauterine system on angiogenic growth factors in the endometrium. 2003
Sep;18(9):1809-19.
7. Marions L,
Hultenby K, Lindell I, Sun X, Stabi B, Gemzell Danielsson K.
Emergency
contraception with mifepristone and levonorgestrel: mechanism of action.
Obstet Gynecol. 2002
Jul;100(1):65-71.
Estudios que no encuentran el tercer mecanismo con el uso de LNG
1. Marta
Durand, Ma. Del Carmen Cravioto,
Elizabeth Raymond, Ofelia Durßn-Sßnchez, Ma. De la Cruz-Hinojosa, Andrķs
Castell-Rodriguez, Rafaela Schiavon, Fernando Larrea. On the mechanism of action
of short-term levonorgestrel administration in emergency contraception.
Contraception 64 (2001)
227-234.
2. Muller AL,
Llados CM, Croxatto HB. Postcoital treatment with
levonorgestrel does not disrupt postfertilization events in the rat.
Contraception.
2003 May;67(5):415-9.
3. Swahn ML,
Westlund P, Johannisson E, Bygdeman M. Effect of post-coital contraceptive
methods on the endometrium and the menstrual cycle. Acta Obstet Gynecol Scand.
1996 Sep;75(8):738-44.
4. Ortiz ME,
Ortiz RE, Fuentes MA, Parraguez VH, Croxatto HB. Post-coital administration
of levonorgestrel does not interfere with post-fertilization events in the
new-world monkey Cebus apella. Hum Reprod. 2004
Jun;19(6):1352-6.
Otros Documentos Anexados
1.
Taskin O, Brown RW, Young
DC, Poindexter AN, Wiehle RD. High doses of oral contraceptives do not alter
endometrial alpha 1 and alpha v beta 3 integrins in the late implantation
window. Fertil Steril. 1994 May;61(5):850-5.
2. Raymond
EG, Lovely LP, Chen-Mok M, Seppala M, Kurman RJ, Lessey BA. Effect of the Yuzpe
regimen of emergency contraception on markers of endometrial receptivity. Hum
Reprod. 2000 Nov;15(11):2351-5.
3. FDA, Plan
B
4. Inserto
del Levonorgestrel Aprobado por la FDA
5. WomenÆs
Capital Corporation. Briefing Document Nonprescription Drugs and Reproductive
Health Drugs Advisory Committee Meeting, 16 December 2003. PLAN B
(Levonorgestrel) for Emergency Contraception Rx-to-OTC Switch. 14 November
2003.
6. Otros
Insertos de Levonorgestrel.
7. La
Anticoncepci¾n de Emergencia, Defensoria del Pueblo, Informe No.
78
8.
International Consortium for Emergency Contraception, Emergency
Contraceptive Pills: Medical and Service Delivery Guidelines Second Edition.
2003.
9. WHO
Essential Medicines Library,Contraception-Emergency,
Levonorgestrel.
10. Informe Tķcnico de la Direcci¾n
General de Salud de las Personas, elaborado por el Dr. Luis
Tßvara
I. Introducci¾n
En el Per·, el
debate sobre la Anticoncepci¾n Oral de Emergencia (AOE) sigue abierto y
constituye un tema de actualidad. La discusi¾n se ha venido centrando sobre la
capacidad de este tipo de sustancias quĒmicas de actuar mediante un mecanismo
antianidatorio o antiimplantatorio. Este mecanismo convierte a este tipo de
drogas en abortivas, dado que tendrĒan la capacidad de impedir la anidaci¾n del
embri¾n humano ¢llamado com·nmente ō¾vulo fecundadoö- en el endometrio, causando
asĒ la muerte de un concebido.
La AOE comprende
una amplia gama de fßrmacos entre los que se encuentran esquemas combinados
estroprogestĒnicos (etinilestradiol y levonorgestrel), progestina sola
(levonorgestrel), antiprogestina sintķtica (mifepristone) y estr¾genos solos en
altas dosis (etinilestradiol).
Existen diversos
mecanismos por los cuales estos fßrmacos evitan o interrumpen el embarazo. El
primer mecanismo act·a sobre la ovulaci¾n, evitßndola o retrasßndola. El segundo
mecanismo es el que act·a sobre la migraci¾n espermßtica, ya sea por el
espesamiento del moco cervical o por la acci¾n directa sobre el espermatozoide,
alterando su capacidad de fecundar. Si estos dos mecanismos no funcionan, y el
espermatozoide ha fecundado el ¾vulo, existe un tercer mecanismo mediante el
cual los fßrmacos utilizados en la AOE alteran el endometrio uterino, evitando
que se implante en ķl el ¾vulo fecundado.
El levonorgestrel en dosis de 0.75mg
tomado dos veces, es un esquema de anticoncepci¾n de emergencia. Hasta la fecha
se considera que los mecanismos de acci¾n de este esquema son los tres descritos
anteriormente. Sin embargo, en el debate en curso el Ministerio de Salud ha
sostenido ¢respaldado por un informe tķcnico-cientĒfico basado en resultados de
estudios experimentales realizados en mujeres en los ·ltimos a±os- que los
mecanismos de acci¾n de la AOE son s¾lo anteriores a la fecundaci¾n. En varias
ocasiones la titular del portafolio, la Dra. Pilar Mazzetti, ha afirmado que
para el levonorgestrel estß cientĒficamente demostrado que el mecanismo
modificador del endometrio -y por tanto el efecto antianidatorio- no
existen.
Con el ßnimo de
contribuir al debate cientĒfico sobre el tema, el Comitķ de Bioķtica de la
Conferencia Episcopal Peruana ha elaborado este informe que recoge y analiza la
evidencia cientĒfica de los ·ltimos a±os (hasta el 2004) respecto al tema. La
informaci¾n ha sido estructurada siguiendo las dos condiciones cuyo supuesto
cumplimiento permitieron que el Ministerio de Justicia modificara su opini¾n
respecto a la AOE, declarßndola conforme a ordenamiento jurĒdico nacional
(oficio N. 516-2004-JUS/DM).
El estado actual
de la medicina ha demostrado que los efectos de la AOE hormonal no pueden ser
·nicamente anticonceptivos. Por otra parte, no existe ning·n estudio ni reciente
ni antiguo que demuestre cientĒficamente que la AOE no ocasiona cambios en el
endometrio y que por lo tanto no impide la anidaci¾n o la implantaci¾n del
concebido. Por ello, en la actualidad, en el ßmbito cientĒfico, el efecto
antianidatorio o antiimplantatorio no ha dejado de ser considerado.
Instituciones como la Organizaci¾n Mundial de la Salud, la Food and Drugs
Administration de los Estados Unidos, y la Gedeon Ritcher, laboratorio
fabricantes y comercializador de levonorgestrel en diferentes paĒses, son
ejemplos claros de la vigencia de dicha informaci¾n
cientĒfica.
II. Preliminares
A. Condiciones requeridas por el Ministerio de Justicia
Primer condicional:
ōSi el estado actual de la medicina ha
determinado que los ·nicos efectos de la AOE son
anticonceptivosö
Segundo
condicional:
ōSi existen estudios suficientes y
actuales que demuestran que la AOE ¢ingerida en la dosis recomendada- no
ocasiona cambios en el endometrio que impidan la anidaci¾n o la
implantaci¾nö.
Solamente si se
cumplen estas dos condiciones ōpuede concluirse que se trata de un mķtodo no
abortivo y que su inclusi¾n en las Normas de Programa Nacional de Planificaci¾n
Familiar es constitucional.
B. Los
mecanismos de acci¾n del levonorgestrel 0.75mg:
Inhibir o retrasar la ovulaci¾n, que
llamaremos en lo sucesivo ōprimer mecanismoö.
Formar un tap¾n
de moco en el cuello uterino o cervix. Lo llamaremos en lo sucesivo ōsegundo
mecanismoö
Alterar el
endometrio impidiendo asĒ la implantaci¾n o anidaci¾n del embri¾n humano
(llamado com·nmente ō¾vulo fecundadoö) en el ·tero. Lo llamaremos ōtercer
mecanismoö. Es la existencia de este mecanismo la que ha sido puesta en duda y
sobre ķl se ha centrado el debate sobre la AOE.
III. Sobre la
primera condici¾n puesta por el Ministro de Justicia:
ōSi el estado actual de la medicina ha
determinado que los ·nicos efectos de la AOE son
anticonceptivosö
Para demostrar
que esta condici¾n no se cumple citaremos informaci¾n cientĒfica que demuestra
que el primer y el segundo mecanismos -juntos o cada uno de manera individual-
no son suficientes para explicar que no se produzca el embarazo en todos los
casos en que se usa levonorgestrel.
A. La Evidencia
Experimental.
La Organizaci¾n Mundial de la Salud (OMS)
ha publicado dos estudios de gran magnitud. El primero de ellos, (WHO Task Force
on Postovulatory Methods of Fertility Regulation, 1998) involucr¾ 1998 mujeres
de 21 centros de investigaci¾n diferentes distribuidos por el mundo y sigui¾ un
dise±o randomizado doble ciego.
Los resultados del estudio vienen
mostrados en la grßfica presentada a continuaci¾n.
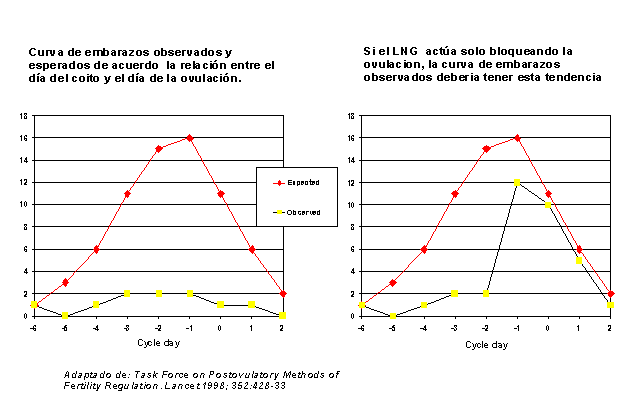
La lectura de
las curvas permite concluir de manera clara que el levonorgestrel act·a no
solamente mediante mecanismos preovulatorios ¢el primer mecanismo-, sino tambiķn
mediante uno o mßs mecanismos postovulatorios, (es decir cuando el ¾vulo ha sido
ya liberado a la trompa de Falopio). Se podrĒa presentar entonces como
responsable de la disminuci¾n en la tasa de embarazos esperados el segundo
mecanismo. Al respecto, vale la pena repasar los hechos biol¾gicos que se
verifican en las relaciones sexuales humanas -mßs especĒficamente, en relaci¾n a
la migraci¾n y capacitaci¾n espermßtica y el efecto que sobre ambas puede tener
el levonorgestrel- y el tiempo en que se puede verificar la
fecundaci¾n:
Es conocido por
la ciencia que el espermatozoide puede demorar s¾lo 5Æ minutos en llegar al
extremo distal de la trompa (Gordon JD, 2002; FIGO, 1994). A ello se suma las
2h. que toma el espermatozoide en capacitarse para fecundar el ¾vulo (Gordon JD,
2002; FIGO, 1994). Ademßs seg·n lo se±ala Kesser³ -en el ·nico estudio sobre el
segundo efecto- el tap¾n de moco se forma despuķs de 9 horas de la toma de
levonorgestrel (Kesser³, 1974). Debemos considerar ademßs el tiempo promedio
¢once (11) horas- que en el mejor de los casos pasa desde la llamada relaci¾n
sexual ōsin protecci¾nö hasta la primera toma de levonorgestrel (Gold MA, 2004).
Todo esto sumado hace que el segundo mecanismo en situaciones reales, sea
limitado y por tanto insuficiente para que pueda ser postulado como el ·nico
responsable de todo el efecto postovulatorio del
levonorgestrel.
El siguiente grafico ayuda a comprender
esto
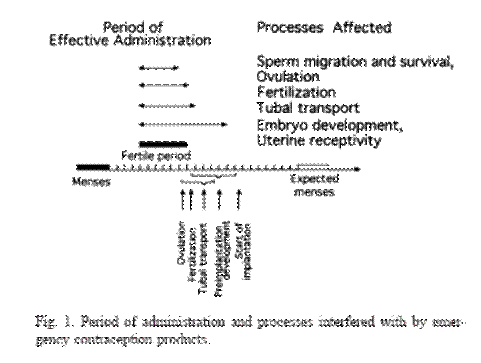
(Croxatto HB, 2001)
En conclusi¾n,
cabe pensar y debe postularse la hip¾tesis cientĒfica de otro u otros efectos
postovulatorios para el levonorgestrel.
El segundo gran
estudio de la OMS (Von Hertz, 2002) involucr¾ 4136 mujeres de 15 clĒnicas de
planificaci¾n familiar en 10 paĒses diferente; tambiķn tuvo un dise±o doble
ciego randomizado.
Entre los
resultados de este estudio se encuentra que el levonorgestrel es efectivo a·n
120 h. despuķs de la toma de la sustancia. ōeven if a declining trend
in efficacy with time were verified, the regimens studied still prevent a high
proportion of pregnancies even up to 5 days after coitusö. Ello muestra
desde otra perspectiva que existe un mecanismo de acci¾n postovulatorios que no
pueden ser explicados por el segundo mecanismo.
B. recogida por
la comunidad cientĒfica.
La conclusi¾n a la que hemos llegado es
recogida por la comunidad cientĒfica en los artĒculos de revisi¾n (ōreviewsö)
sobre la AOE de los ·ltimos cinco a±os, que respecto a los mecanismos de acci¾n
afirman unßnimemente la misma idea expresada con diferentes palabras: no se
conoce todo sobre los mecanismos de acci¾n del levonorgestrel. Ademßs en ninguno
de ellos se niega la existencia del tercer mecanismo alterador del endometrio
uterino.
ōHowever, the knowledge of the mechanism
of action of mifepristone and levonorgestrel in humans, when used for
contraceptive purposes and especially for emergency contraception, remains
incomplete.[...]. The contraceptive effects of both levonorgestrel and
mifepristone, [...] involve either blockade or delay of ovulation, due to either
prevention or delay of the LH surge, rather than to inhibition of implantationö
(Gemzell-Danielsson K, 2004);
ōThe mode of action of levonorgestrel
emergency contraception is to prevent or delay ovulation and/or alter the
endometrium unfavourably for the implantation of an embryoö (Sarkar,
2003);
ōThe issue is whether they act by
preventing fertilization or by impeding the successful development of the zygote
through and beyond implantation. Until now, published works has left this issue
largely unresolved, and this paucity of knowledge sustains heated controversies
in many settings [...] The exact mode of action of HEC remains undeterminedö
(Croxatto, 2003);
The 2 most
common types of hormonal EC used in the US are the Yuzpe regimen (high-dose
ethinyl estradiol with high-dose levonorgestrel) and Plan B (high-dose
levonorgestrel alone). Although both methods sometimes stop ovulation, they may
also act by reducing the probability of implantation, due to their adverse
effect on the endometrium (a postfertilization effect). The available evidence
for a postfertilization effect is moderately strong, whether hormonal EC is used
in the preovulatory, ovulatory, or postovulatory phase of the menstrual cycle.
CONCLUSIONS: Based on the present theoretical and empirical evidence, both the
Yuzpe regimen and Plan B likely act at times by causing a postfertilization
effect, regardless of when in the menstrual cycle they are used. (Kahlenborn,
2002);
"Several studies
have shown histological or biochemical alterations in the endometrium after
treatment with this regimen, suggesting that it may impair endometrial
receptivity to implantation of a fertilized egg (5 ref.). However, other studies
(3 ref.) have found no such endometrial effects. Whether the endometrial changes
that have been observed would be sufficient to inhibit implantation remains
unclear". (Grimes, 2002);
ōIt can delay or
prevent ovulation, impair formation of the corpus luteum, or cause histological
or biochemical changes within the endometrium, thus preventing implantationö
(Pham, 2002);
ōEstrogen and progesterone, alone or in
combination, inhibit or delay ovulation. However, in human studies the evidence
is less clear about cumulative effects on fertilization, gamete transport, the
endometrium, functioning of the corpus luteum or implantation.ö (Wertheimer,
2000).
En otras palabras, podemos concluir que
no existe consenso cientĒfico para descartar el tercer mecanismo de acci¾n del
LNG. Ning·n estudio a la fecha ha demostrado que el tercer mecanismo del
levonorgestrel no exista.
IV. Sobre la
segunda condici¾n puesta por el Ministro de Justicia.
ōSi existen estudios suficientes y
actuales que demuestran que la AOE ¢ingerida en la dosis recomendada- no
ocasiona cambios en el endometrio que impidan la anidaci¾n o la
implantaci¾nö.
Para demostrar
que esta condici¾n no se cumple hay que analizar a su vez dos cosas: que existen
estudios publicados en la literatura cientĒfica que sĒ encuentran cambios en el
endometrio; y que los estudios que han sido presentados como que ōdemuestran
claramente que la AOE no tiene efecto sobre el endometrio, y como consecuencia
su mecanismo de acci¾n no estß a ese nivelö, en realidad no son
demostrativos.
A. Estudios cientĒficos sĒ encuentran cambios endometriales
En la literatura cientĒfica de los
·ltimos 30 a±os se pueden hallar varios estudios en los que se reportan cambios
endometriales causados por el levonorgestrel. Ello permite afirmar que
hist¾ricamente, en medicina, al levonorgestrel se le ha reconocido siempre el
mecanismo de acci¾n alterador del endometrio. A continuaci¾n presentamos
aquellos mßs representativos. Como es reconocido por todos los cientĒficos
investigadores del argumento, los cambios en el endometrio interfieren con la
anidaci¾n o implantaci¾n de embri¾n humano (el llamado ō¾vulo
fecundadoö).
El estudio
clßsico de Moggia y colaboradores (Moggia A., 1974) sigui¾ una cohorte de 314
mujeres que completaron un promedio de 4.3 ciclos de D-norgestrel (isomero) con
dosis menores a las usadas actualmente, 0.35mg en una sola toma, 255 pacientes
completaron el estudio. Se tomaron biopsias de endometrio alrededor del dĒa 14
del ciclo en 92 pacientes que usaron este producto entre 6 y 10 veces por ciclo.
En 76 pacientes (82%, intervalo de confianza 74.2%-89.8%), se observ¾ un
endometrio secretorio irregular y en casi todas las participantes biopsiadas se
encontr¾ corona de linfocitos alrededor de la glßndulas. De este estudio se
puede concluir que en el 82% de pacientes se encontraron cambios significativos
en el endometrio en personas que usaron este producto entre 6 y 10 veces por
ciclo.
Ugocsai y
colaboradores (Ugocsai G., 1984) encuentran alteraciones endometriales al
evaluar conejos que recibieron distintas dosis de D-norgestrel. Se encontr¾
ademßs que la intensidad de los cambios dependĒa de la dosis, evidenciando una
relacion dosis-respuesta. La conclusi¾n del artĒculo
es muy sugerente: ōIt can be suggested that d-norgestrel alters the surface of
the endometrium to such an extent that nidation is unable to take place;
therefore, it can be used for postcoital contraception at any timeö.
Este mismo autor repite su
experimento en el a±o 2002 en humanos (Ugocsai G., 2002). En este estudio tres
mujeres toman dosis de levonorgestrel superiores a las recomendadas (dos a tres
veces mßs) y dos mujeres son tomadas como casos controles. La microscopia
electr¾nica mostr¾ claramente cambios en las 3 personas que tomaron la hormona
sintķtica.
Landgren y
colaboradores (Landgren BM, 1989) describen cambios menores en el endometrio en
un estudio que involucr¾ 10 personas que recibieron levonorgestrel
0.75.
Shirley y
colaboradores (Shirley B., 1995) muestran contundentemente que el efecto de
alteraci¾n del endometrio causado por el LNG se traduce en un efecto
directamente abortivo. En este estudio se encontraron embriones momificados en
ratas en las que se colocaron implantes de liberaci¾n continua de LNG despuķs
del periodo de apareamiento. En ese sentido, Roopa y col, refieren encontrar
factores que pueden estar involucrados en la angiogenesis aberrante en el
endometrio de mujeres que usan dispositivos uterinos que libera dosis peque±as
de levonorgestrel (Roopa 2003).
Marions en un
studio en que usa el LNG 0.75 en dos tomas (Marions L., 2002), encontr¾ que una
de cuatro mujeres evaluadas mediante biopsia endometrial presentaba alteracion
en uno de los indicadores estudiados (COX-2). A pesar de las limitaciones que
este estudio presenta, sobre lo cual nos detendremos a continuaci¾n, esta
investigaci¾n constituye una prueba adicional del efecto del LNG sobre el
endometrio.
B. Los artĒculos
citados en el debate sobre el mecanismo de acci¾n del levonorgestrel no
demuestran que la AOE no tenga efecto sobre el endometrio
El informe Tßvara -apreciaci¾n tķcnica en
la cual se basa la ministra para hacer sus afirmaciones y definir las polĒticas-
cita solamente cuatro artĒculos que eval·an el levonorgestrel para afirmar que
ōdemuestran claramente que la AOE no tiene efecto sobre el endometrio y como
consecuencia su mecanismo de acci¾n no estß a ese nivelö. Ahora nos detenemos a
estudiar dichos experimentos.
El estudio de
Marions y colaboradores (Marion L., 2002) estudiaron 6 mujeres que recibieron
levonorgestrel. De ellas s¾lo 4 pudieron ser analizadas mediante biopsia
endometrial. Esto significa que los investigadores perdieron el 33% de su
muestra original lo cual desde el punto de vista estadĒstico perjudica mucho las
conclusiones de un estudio. El estudio ademßs se±ala que en una de las biopsias
estudiadas sĒ se encontr¾ modificaciones en un marcador estudiado (COX-2). El
informe Tavara, sin embargo, no menciona nada de esto y mßs a·n afirma que
ōninguno de estos parßmetros [evaluados por Marions] mostr¾ diferencias con lo
observado en las biopsias obtenidas en los ciclos control (sin AOE) de las
mismas mujeresö. En otras palabras, omite decir que el estudio sĒ encuentra
cambios en el endometrio. Ademßs un estudio con cuatro unidades de anßlisis es
por demßs insuficiente para descartar la posibilidad de no encontrar diferencias
donde si las hay, (lo que se conoce en estadĒstica como ōerror tipo IIö). Los
autores aceptan las limitaciones de su propia investigaci¾n y no descartan en
ning·n momento la posibilidad de que el levonorgestrel afecte el endometrio: ōIn
conclusion, our data suggest that the ovulation process is the main target for
emergency contraception with mifepristone and levonorgestrel.ö. El informe
Tßvara, sin embargo, lo cita como su primera evidencia que demuestra que el
levnorgestrel no altera el endometrio, algo que ni los mismos autores concluyen
en su estudio.
El segundo
estudio es el de Durand y colaboradores (Durand M, 2001). El n·mero de mujeres
incluĒdas en el estudio es mayor al de Marions, sin embargo presenta serias
deficiencias metodologicas. Primeramente, no refiere que la asignaci¾n a los
grupos de estudio hayan sido hechos la azar, esto le resta poder demostrativo al
estudio. En segundo lugar, no se respeta la asignaci¾n original a cada grupo lo
que altera todavĒa mßs la calidad del estudio. Una tercera deficiencia del
estudio es que en el dise±o original se debi¾ analizar 33 controles, sin embargo
solo se evaluaron 24, es decir se perdieron el 27% de sus casos, lo cual tambien
representa una seria deficiencia para llegar a conclusiones vßlidas. Finalmente,
como en el estudio anterior, la muestra es demasiado peque±a para descartar
consistentemente el error tipo II. Nuevamente en el informe Tßvara se le
atribuye al estudio un valor que ni sus mismos autores le otorgan para negar la
existencia del tercer mecanismo. Durand y colaboradores
concluyen: Our results may offer a plausible explanation for the contraceptive
effects of LNG given postcoitally prior to LH surge or the mechanism involving
corpus luteum development. In addition, this study does not support an
antiimplantation contraceptive effect of LNG in EC; however, additional targets,
besides those described herein, should also be considered and further
investigated for the contraceptive effects of LNGö. Los autores en ning·n
momento afirman haber demostrado que no existe el tercer mecanismo; sin embargo,
el infome Tßvara lo cita como la segunda evidencia que cierra la discusi¾n sobre
tercer mecanismo del LNG, porque demostrarĒa que este no
existe.
A la luz de las
estßndares exigidos actualmente por la medicina basada en evidencias, el poder
demostrativo de estos dos estudio es insuficiente.
El informe
Tßvara prosigue mencionando que ōexisten estudios experimentales en animales que
han contribuido a aclarar el mecanismo de acci¾n del LNGö. Antes de pasar a
examinar cada uno de ellos cabe mencionar que los modelos animales tienen
limitaciones para ser extrapolables a los humanos y seg·n refiere la FDA solo el
20% de las drogas probadas en animales tienen mecanismos semejantes en
humanos.
Si bien el rigor
cientĒfico del estudio que Muller y colaboradores (Muller A.L., 2003) realizaron
en ratas es aceptable, su extrapolaci¾n al modelo humano es dudoso, ya que usa
una dosis varias veces mayor que la sugerida para humanos y toma como indicador
indirecto el porcentaje de fecundaci¾n. Si consideramos a las ratas como modelos
para probar esta hip¾tesis tendrĒamos que considerar tambiķn el estudio de
Shirley y colaboradores (Shirley B., 1995) en el que se encontraron embriones
momificados como evidencia de la acci¾n post ovulatoria y abortiva de
Levonorgestrel, o el de Ugocsai y colaboradores (Ugocsai G., 1984) que encontr¾
cambios endometriales a la microscopia electr¾nica en conejos. Pero el informe
Tßvara no ha tenido en cuenta estos estudios.
El segundo
estudio en animales que menciona corresponde a un experimento realizado en monos
Cebus apella por Ortiz y colaboradores (OrtĒz M.E., 2004). De la lectura del
artĒculo se puede concluir que los hallazgos del experimento han sido
interpretados con mucha libertad por los investigadores al momento de decidir el
tĒtulo del artĒculo. El estudio eligi¾ la tasa de embarazos como indicador
indirecto del efecto anticonceptivo y no encontr¾ diferencias en la proporci¾n
de embarazos cuando el levonorgestrel postcoital actu¾ antes o despuķs de la
ovulaci¾n. En otras palabras, en esta especie animal el levonorgestrel
postcoital no s¾lo no interfiere con los eventos post-fertilizaci¾n -como lo
resalta el tĒtulo del artĒculo- sino que tampoco interfiere con los eventos
pre-ovulatorios. Entonces, la sustancia no tendrĒa efecto alguno en este modelo
animal, tal como lo reconocen los mismos autores en la conclusi¾n del estudio:
ōel LNG administrado despuķs del coito, no previene el embarazo de esta especie
primate, aparentemente porque el C. apella tiene un patr¾n de apareamiento
distinto al de los humanosö. Los resultados de este estudio tampoco son
extrapolables a humanos. Sin embargo el informe Tavara presenta este estudio
como uno de los que demustra de manera concluyente que en las mujeres el tercer
mecanismo del LNG no ocurre.
C. Deficiencias del Informe Tßvara
Hay otras observaciones y crĒticas que
hacerle al informe Tßvara, dado que es el sustento cientĒfico que fundamenta la
solicitud que la Ministra de Salud hace al Ministerio de Justicia para que
modifique su dictamen sobre la inconstitucionalidad de la
AOE.
Ya hemos llamado
la atenci¾n sobre el uso poco objetivo de las publicaciones cientĒficas para
ordenarlas a la idea que el informe propone es decir que estarĒa demostrado
cientĒficamente que el Levonorgestrel no afectarĒa el endometrio. Ello se nota
una vez mßs en la pßgina 8. Citando el estudio de Taskin y colaboradores (Taskin
O., 1994. Ver anexo 22) el informe dice ōencontraron que en biopsias de
endometrios de mujeres que habĒan recibido altas dosis de anticonceptivos orales
no se alteraban las alfa-1 y las beta-3 integrinas, que son citoquinas
necesarias para el proceso de implantaci¾n del blastocisto en el endometrio.ö
Sin embargo, no se menciona que en este estudio participaron s¾lo 3 mujeres, por
lo cual el valor demostrativo de este estudio es casi inexistente. Compßrese,
por ejemplo, con el volumen de pacientes estudiados en los dos estudios de la
OMS que hemos citado al inicio.
Siempre en la
pag. 8 se lee: ōSwahn en Europa en Europa (1996) y Raymond en los Estados Unidos
(2000) examinaron biopsias de endometrio tomadas en el periodo supuestamente de
implantaci¾n en mujeres que tomaron AOE seg·n el rķgimen de Yuzpe y no
encontraron diferencias significativas en los parßmetros morfol¾gicos y
moleculares examinados, cuando fueron comparados con los ciclos control (sin
AOE) en las mismas mujeres.ö
Sobre estos dos
articulos es importante hacer notar lo siguiente. El estudio de Swahn y
colaboradores (Ver anexo 20) no es contundente al negar el efecto de
modificaci¾n endometrial y dice textualmente: ōThe findings indicate that the
contraceptive effect of postcoital treatment with EE/LNG and danazol is mainly
due to an inhibition or delay of ovulation and insufficient corpus luteum
function. The direct effect on the endometrium is limited, if anyö. AsĒ queda claro
que se ha hecho una interpretacion arbitraria de este estudio para afirmar
categ¾ricamente que no se producen cambios en el endometrio, cosa que ni los
mismos autores del estudio se atreven a afirmar.
La manipulaci¾n
al presentar los hallazgos del estudio de Raymond y colaboradores (Ver anexo 23)
es a·n mas evidente, ya que cinco de los nueve indicadores investigados ¢es
decir, la mayorĒa- sĒ experimentaron alteraciones. El mismo autor se±ala: ōWe
did note five statistically significant differences in treated cycles compared
with untreated cycles: a reduction in endometrial MUC-1 expression, an increase
in endometrial ER, lower luteal phase serum oestrogen concentration, reduced
endometrial thickness, and greater proportion of glandular supranuclear
vacuolesö. El informe Tavara toma s¾lo
una parte de los hallazgos de estos investigadores ¢aquella que conviene a la
idea que quiere concluir- y omite mencionar que cinco parametros endometriales
sĒ cambiaron. Sorprendentemente es presentado como demostrativo de que el mķtodo
Yuzpe no produce cambios en el endometrio.
Es importante
rescatar los comentarios de Raymond y colabradores respecto a los dos estudios
citados anteriormente. Sobre el estudio de Taskin
y col. observa que ōNo disturbances of integrin expression were found, [...].
However, [...] the treatment was given long after the end of the fertile period,
when the regimen would not be expected to be effective, and the proteins may not
have been evaluated on the appropriate day f the luteal phaseö. Es decir, por el
error de dise±o del estudio no era de esperarse que el endometrio resultara
modificado. Ello hace perder validez cientĒfica al estudio de Taskin.
Respecto a la investigaci¾n
de Swahn y colaboradores dice: ōIn contrast, a more recent study found no
endometrial phase abnormalities in eight women treated 2 days after the LH surge
(Swahn, 1996). That study did find significantly more vacuolated cells (similar
to our results) and wider diameters of gland lumina, but the authors interpreted
these effects as clinically insignificant.ö En otras palabras, Raymond
reconoce que Swahn sĒ encuentra cambios morfol¾gicos en el endometrio, incluso
mayores que los suyos, aunque los autores hagan despuķs una interpretaci¾n
personal del hallazgo objetivo de su investigaci¾n.
N¾tese que los
estudios que acabamos de citar no se refieren al fßrmaco en cuesti¾n -el
levonorgestrel- sino al mķtodo Yuzpe. Sin embargo, el informe Tßvara se vale de
esta informaci¾n -que como hemos visto es presentada de manera poco objetiva-
para introducir la idea de que la AOE ¢dentro de la cual se incluye aquella con
levonorgestrel- no produce cambios en el endometrio.
Hay que
mencionar que existen estudios que demuestran categ¾ricamente el efecto del
rķgimen Yuzpe sobre el endometrio. Quizß el mßs representativo es el de Trussell
y Raymond (Trussell J., 1999). En ese estudio los autores presentan evidencia
estadĒstica sobre el mecanismo de acci¾n del mķtodo de Yuzpe, y concluyen que el
mecanismo de acci¾n de los estroprogestĒnicos no puede ser explicado solamente
por la inhibici¾n de la ovulaci¾n. Pero esa informaci¾n tambiķn es omitida por
este informe tķcnico. Como hemos visto, Raymond encuentra cambios en varios
parametros endometriales luego de la suministraci¾n del protocolo de Yuzpe, y no
es el ·nico en la literatura cientĒfica. Se ha reportado que el protocolo de
Yuzpe reduce el n·mero de receptores para los estr¾genos y para la progesterona
si se suministran 48 horas despuķs del pico de LH (Kubba A., 1986). Otros
estudios han encontrado que causa tambiķn un desarrollo asincr¾nico del
endometrio, generando un ambiente que los investigadores consideran inadecuado
para la implantaci¾n del embri¾n ( Yuzpe A., 1974; Ling W.Y., 1983). A la misma
conclusi¾n se llega cuando se suministra el protocolo de Yuzpe en fase
preovulatoria (Ling W.Y., 1983).
V. Otras Opiniones a Considerar
La FDA a la fecha tampoco acepta que el
efecto modificador sobre el endometrio estķ descartado. De la misma posici¾n son
los fabricantes del fßrmaco (la Gedeon Ritcher, diciembre 2003) y la
OMS.
La opini¾n de la
FDA, debe ser considerada necesariamente en este debate. Los estudios recogidos
por la FDA en diciembre del 2003 no dan cuenta de investigaciones que determinen
que el tercer efecto haya sido descartado. Por el contrario la ·ltima
comunicaci¾n oficial de la FDA hecha el 7 de mayo de 2004 (Ver anexo 24)
reconoce todavĒa la existencia del tercer mecanismo. El inserto aprobado por la
FDA lo establece claramente (Ver Anexo 25).
Fue la Directora
de la Divisi¾n de Investigaci¾n de los Laboratorios Barr, que comercializa la
droga en los Estados Unidos, quien present¾ a la FDA, en el contexto del debate
acerca de la venta sin receta del LNG 0.75 en Estados Unidos, un informe
cientĒfico con una propuesta de inserto que no oculta la posibilidad de este
tercer mecanismo (Ver Anexo 26).
Los que
comercializan esta droga en paĒses en donde el aborto es legal o se considera
aborto la interrupci¾n del embarazo s¾lo despuķs del momento de la implantaci¾n,
tampoco tienen necesidad de ocultar esta informaci¾n y la consideran en los
insertos. (Ver Anexo 27)
En el Per· los
fabricantes no han solicitado un cambio oficial del inserto. La informaci¾n
disponible en ese sentido es una comunicaci¾n de la DefensorĒa de Pueblo que
adjunta una carta de Teodora Perger, funcionaria de Gedeon Richter en la que da
su opini¾n acerca de los modos de acci¾n del levonorgestrel cuestionando el
tercer mecanismo (Ver Anexo 28). Sin embargo la misma funcionaria form¾ parte de
un comitķ cientĒfico que en el mismo a±o 2003 pubica una guĒa de anticoncepci¾n
de emergencia en la que se reconoce abiertamente la existencia del mecanismo
antiimplantatorio (Ver anexo 29).
Finalmente cabe
se±alar que la OMS nunca ha negado la existencia del tercer mecanismo y lo
reconoce abiertamente en la informaci¾n disponible en su pagina web (WHO
Essential Medicines Library) (Ver anexo 30).
Creemos que
existe evidencia cientĒfica que sostiene la hip¾tesis que el Levonorgestrel 0.75
mg x 2 tiene un tercer mecanismo que altera el endometrio y evita la
implantaci¾n del ¾vulo fecundado y que los estudios recientes tanto en humanos
como en animales son escasos e insuficientes para demostrar lo contrario. Asi lo
expresan contundentemente las ·ltimas revisiones publicadas por expertos en el
tema, lo mismo es sostenido abiertamente por la FDA, por la Gedeon Ritcher (los
fabricantes de esta droga) y por la OMS.
VI.
Conclusi¾n:
El estado actual de la medicina ha
demostrado que los efectos de la AOE hormonal no pueden ser ·nicamente
anticonceptivos. Esto ha sido evidenciado estadĒsticamente en el caso del
protocolo de Yuzpe; y se desprende de los resultados de estudios multicķntricos
de la OMS para el caso del levonorgestrel. Por otra parte, no existe ning·n
estudio ni reciente ni antiguo que afirme haber demostrado cientĒficamente que
la AOE no ocasiona cambios en el endometrio y que por lo tanto no impide la
anidaci¾n o la implantaci¾n del concebido. Otros estudios sĒ reportan
modificaciones en el endometrio por efecto del levonorgestrel solo o combinado
con estroprogestĒnicos, usado como AOE. Por ello, en la actualidad, en el ßmbito
cientĒfico, el efecto antianidatorio o antiimplantatorio ¢especialmente para el
levonorgestrel 0.75- no ha dejado de ser reconocido p·blicamente. Instituciones
como la Organizaci¾n Mundial de la Salud, la Food and Drugs Administration de
los Estados Unidos, y la Gedeon Ritcher, laboratorio fabricantes y
comercializador de levonorgestrel en diferentes paĒses, son ejemplos claros de
la vigencia de dicha informaci¾n cientĒfica; ello no quita que algunos
investigadores duden de la existencia de dicho efecto antiimplantatorio.
Finalmente, existe consenso en la comunidad cientĒfica para afirmar que el
mecanismo de acci¾n del levonorgestrel a·n no estß totalmente esclarecido, en
especial en lo relacionado a sus mecanismos postovulatorios. Por lo tanto,
concluimos que desde el punto de vista cientĒfico, no se cumplen ninguna de las
dos condiciones puestas por el Ministerio de Justicia para declarar
constitucional la Anticoncepci¾n Oral de Emergencia.
VII. Bibliografia
Croxatto HB, Devoto L, Durand M, Ezcurra
E, Larrea F, Nagle C, Ortiz ME, Vantman D, Vega M, von Hertzen H. Mechanism of
action of hormonal preparations used for emergency contraception: a review of
the literature. Contraception. 2001 Mar;63(3):111-21.
Review.
Croxatto HB,
Ortiz ME, Muller AL., Steroids. Mechanisms of action of emergency contraception.
2003 Nov;68(10-13):1095-8.
Durand M, del
Carmen Cravioto M, Raymond EG, Duran-Sanchez O, De la Luz Cruz-Hinojosa M,
Castell-Rodriguez A, Schiavon R, Larrea F. On the mechanisms of action of
short-term levonorgestrel administration in emergency contraception.
Contraception. 2001 Oct;64(4):227-34.
FIGO Federacion Internacional de
Ginecologia y Obstetricia, Manual de Reproducci¾n Humana, The Parthenon
Publishing Group, New , New Cork, USA. 1994
Gemzell-Danielsson K,
Marions L., Mechanisms of action of mifepristone and levonorgestrel when used
for emergency contraception. Hum Reprod Update.2004 Jul-Aug;10(4):341-8.
(Abstract).
Gold MA, Wolford
JE, Smith KA, Parker AM. The effects of advance provision of emergency
contraception on adolescent women's sexual and contraceptive behaviors.
J
Pediatr Adolesc Gynecol. 2004
Apr;17(2):87-96.
Gordon JD,
Speroff L. Handbook for Clinical Gynecologic Endocrinology and Infertility,
LIPPINCOTT WILLIAMS & WILKINS, Philadelphia, USA. 2002
Grimes D.A.,
Raymond E., Emergency Contraception. Ann Intern Med 2002 ; 137
:180-9
Kahlenborn C,
Stanford JB, Larimore WL. Postfertilization effect of hormonal emergency
contraception. Ann Pharmacother. 2002 Mar;36(3):465-70.
Kesseru E,
Garmendia F, Westphal N, Parada J. The hormonal and peripheral effects of
d-norgestrel in postcoital contraception. Contraception. 1974
Oct;10(4):411-24.
Kubba A., White
J.O., Guillebaud J. et al., The Biochemistry of Human Endometrium after Two
Regimens of Postcoital Contraception, a D (-) Norgestrel/Ethinylestradiol
Combination or Danazol, Fertil Steril 1986; 45: 5212-516.
Landgren BM, Johanisson E, Aedo AR, Kumar
A, Shi Yong-en. The effect of Levonorgestrel administered in large doses at
different stages of the cycle on ovarian function and endometrial morphology.
Contraception, 39 (3), 1989. 275- 289.
Ling WY, Wrixon
W. Zayid I, et al., Mode of Action of dl-Norgestrel and Ehinylestradiol
Combination in Postcoital Contraception. II. Effect of Postovulatory
Administration on Ovarian Function and Endometrium, Fertil Steril 1983; 39.
292-297.
Ling WY, Wrixon
W, Acorn T, et al., Mode of Action of dl-Norgestrel and Ethinylestradiol
Combination in Postcoital Contraception. III. Effect of Preovulatory
Administration Following the Luteining Hormone Surge on Ovarian Steroidogenesis,
Fertil Steril 1983; 40-631-636.]
Marions L,
Hultenby K, Lindell I, Sun X, Stabi B, Gemzell Danielsson K. Emergency
contraception with mifepristone and levonorgestrel: mechanism of action.
Obstet Gynecol. 2002
Jul;100(1):65-71.
Moggia A,
Beauquis A, Ferrari F, Torrado ML, Alonso JL, Koremblit E, Mischler T. The use
of progestogens as postcoital oral contraceptives. Reprod Med. 1974
Aug;13(2):58-61
Muller AL,
Llados CM, Croxatto HB. Postcoital treatment with
levonorgestrel does not disrupt postfertilization events in the rat.
Contraception. 2003 May;67(5):415-9.
Ortiz ME, Ortiz
RE, Fuentes MA, Parraguez VH, Croxatto HB. Post-coital administration
of levonorgestrel does not interfere with post-fertilization events in the
new-world monkey Cebus apella. Hum Reprod. 2004
Jun;19(6):1352-6.
Ortiz ME, Muller
AL., Steroids. Mechanisms of action of
emergency contraception. 2003 Nov;68(10-13):1095-8.
Pham A.
Emergency contraception (post-coital Contraception), J Okla State Med Assoc.
2002 Jun;95(6):371-4. (Abstract).
Raymond EG,
Lovely LP, Chen-Mok M, Seppala M, Kurman RJ, Lessey BA. Effect of the Yuzpe
regimen of emergency contraception on markers of endometrial receptivity. Hum
Reprod. 2000 Nov;15(11):2351-5.
Roopa BA, Loganath A, Singh K. Hum
Reprod. The effect of a levonorgestrel-releasing intrauterine system on
angiogenic growth factors in the endometrium. 2003
Sep;18(9):1809-19.
Sarkar NN.,
Levonorgestrel as an emergency contraceptive drug. Int J Clin Pract. 2003
Nov;57(9):824-8.
Shirley B,
Bundren JC, McKinney S. Levonorgestrel as a postcoital contraceptive.
Contraception. 1995 Nov;52(5):277-81.
Swahn ML,
Westlund P, Johannisson E, Bygdeman M. Effect of post-coital contraceptive
methods on the endometrium and the menstrual cycle. Acta Obstet Gynecol Scand.
1996
Sep;75(8):738-44.
Taskin O, Brown
RW, Young DC, Poindexter AN, Wiehle RD. High doses of oral contraceptives do not
alter endometrial alpha 1 and alpha v beta 3 integrins in the late implantation
window. Fertil Steril. 1994 May;61(5):850-5.
Trussell J.,
Raymond EG., Statistical evidence about the mechanism of action of the Yuzpe
regimen of emergency contraception, Obstet Gynecol. 1999 May;93(5 Pt
2):872-6
Ugocsai G, Resch
B, Traub A, Sas M., Biological, microscopic and scanning electron microscopic
investigations of the effects of postinor /d-norgestrel/ in rabbits.
Contraception. 1984 Aug;30(2):153-9.
Ugocsai G.,
Pozsa M, Ugocsai P. Scanning electron microscopic (SEM) changes of the
endometrium in women takimg high doses of levonorgestrel as emergency postcoital
contraception Contraception 2002 Dec; 66(6): 433-7.
von Hertzen H,
Piaggio G, Ding J, et al. Low dose mifepristone and two regimens of
levonorgestrel for emergency contraception: a WHO multicentre randomized trial.
Lancet. 2002; 360:1803-1810.
Wertheimer RE. Emergency postcoital
contraception.Am Fam Physician. 2000 Nov 15;62(10):2287-92.
Review.
WHO Task Force
on Postovulatory Methods of Fertility Regulation. Randomised controlled trial of
levonorgestrel versus the Yuzpe regimen of combined oral contraceptives for
emergency contraception. Lancet 1998;352:428-433.
Yuzpe AA, Turlow
HJ, Ramzy I et al., Postcoital Contraception: a Pilot Study, J Reprod Med 1974;
13: 53-61;